科研速递|Nature阿尔茨海默病的新机制——ABCA7基因变异导致的磷脂代谢紊乱与线粒体功能障碍
2025年9月10日,《Nature》发表的一项突破性研究,凭借多组学、单细胞与等基因模型“三位一体”的实验体系,首次系统阐明了ABCA7变异如何通过重塑神经元脂质代谢、耦合线粒体功能,进而驱动阿尔茨海默病(AD)相关病理级联,并同步验证了一款临床可及的干预策略,为解析AD发病机制与精准干预开辟了新视野。

一、研究背景
AD是最常见的神经退行性疾病,其病理特征包括β-淀粉样蛋白(Aβ)沉积、Tau蛋白过度磷酸化、神经元丢失和突触功能障碍。除了APOE ε4等位基因外,全基因组关联研究(GWAS)还发现了多个AD风险基因,其中ABCA7尤为突出。ABCA7是一种ATP结合盒转运蛋白,在大脑的神经元和胶质细胞中表达,参与磷脂跨膜转运、维持细胞膜不对称性和脂质外排。遗传学研究表明:
(1)罕见的功能丧失变异(如无义、移码突变)使AD风险增加约2倍(OR≈2),仅次于APOE ε4。
(2)常见错义变异p.Ala1527Gly(rs3752246)也与AD风险适度相关(OR≈1.15)。尽管ABCA7与AD的遗传关联明确,但其在AD发病中的具体机制,特别是如何通过调控脂质代谢影响神经元功能,仍需进一步研究。
二、研究方法
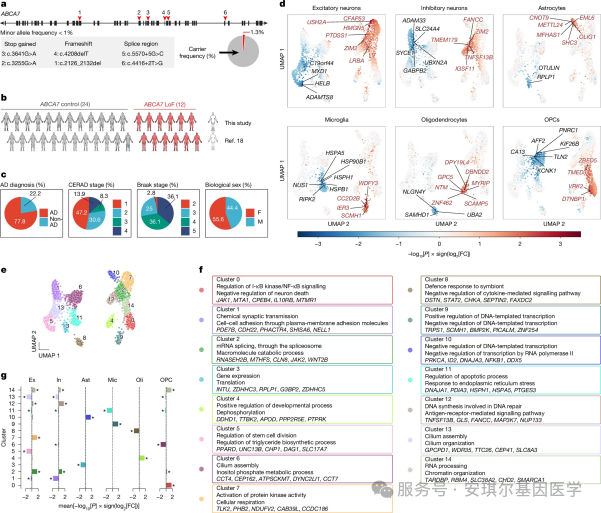
1. 多层次组学整合分析
本研究建立了从人脑组织到体外模型的多层次研究体系,包括:
(1)人脑单核转录组图谱:对ROSMAP队列中12例ABCA7 LoF携带者和24例对照组的前额叶皮层样本进行10x Genomics单核RNA测序,涵盖超过10万个高质量细胞,包括多种神经元和胶质细胞。
(2)iPSC源性神经元模型:使用CRISPR-Cas9技术构建了两株等基因ABCA7 LoF iPSC系(p.Glu50fs*3 和 p.Tyr622),并诱导分化为兴奋性神经元,进行转录组、脂质组、代谢组及功能验证。
(3)皮质类器官模型:通过长期培养(>150天)的皮质类器官,研究Aβ分泌和电生理表型。
2. 跨尺度技术联用
(1)分子动力学模拟:比较ABCA7在Ala1527和Gly1527变异下的结构动态变化(闭合与开放状态),探讨变异如何通过改变局部柔性影响脂质转运。
(2)海马能量代谢分析:使用Seahorse技术测量线粒体耗氧率等参数,评估呼吸功能。
(3)脂质组学与代谢组学:利用LC-MS技术分析多种脂质分子,揭示ABCA7功能丧失引起的脂质组成变化。
三、核心发现
1. ABCA7 LoF引起跨细胞类型的广泛转录紊乱单细胞分析揭示了不同类型的神经细胞对ABCA7功能丧失(LoF)变异的差异化响应:
(1)小胶质细胞:观察到应激反应相关基因表达水平下降,这可能暗示着该类细胞在执行免疫监测功能方面存在缺陷。
(2)星形胶质细胞:转录调控相关的基因表达显著上调,这一现象或与神经炎症过程有关联。
(3)神经元(特别是兴奋性神经元):
DNA修复途径被激活,例如FANCC和RECQL等基因的表达增加;
与突触传递相关的基因表达减少,如NLGN1及SHISA6等;
涉及线粒体氧化磷酸化的基因表达增强;
参与甘油三酯合成过程的基因表达则呈现下调趋势。
2. 兴奋性神经元是ABCA7功能的关键靶点ABCA7在兴奋性神经元中表达水平最高,其功能丧失(LoF)导致以下三个主要变化:
(1)脂质代谢失衡:
饱和磷脂酰胆碱(PC)含量增加,而多不饱和PC(尤其是富含多不饱和脂肪酸的种类)含量减少。
PC合成的关键酶LPCAT3的表达量降低,影响了多不饱和脂肪酸的引入。
长链多不饱和甘油三酯(TG)积累,表明存在脂质储存与利用之间的失调。
(2)线粒体功能障碍:
线粒体解耦联呼吸受损,表现为解耦联比例下降,同时线粒体内膜电位升高。
氧化应激加剧,通过CellROX荧光信号增强得以证实。
线粒体解耦联蛋白UCP2表达量减少,进一步加剧了膜电位升高及活性氧(ROS)生成。
(3)神经元电生理异常:
ABCA7 LoF神经元表现出更高的兴奋性,在较低电流刺激下即可诱发动作电位。
这种现象与AD患者中观察到的神经元过度兴奋特征相一致。
3. 常见变异p.Ala1527Gly模拟部分LoF表型:
(1)携带Gly1527变异的兴奋性神经元在基因表达谱上与功能丧失(LoF)状态呈现出高度相似性,尤其是在涉及DNA损伤应答及线粒体功能的相关基因方面。
(2)分子模拟研究表明,Gly1527变异可能通过增加ATP结合构象中局部结构的灵活性,从而降低ABCA7蛋白介导的脂质外排效率,部分模拟了LoF效应。
四、干预策略
CDP-胆碱补充治疗的多重获益。研究团队对CDP-胆碱(胞磷胆碱)作为潜在的干预手段进行了综合评估,揭示了其多方面的生物学效应:
1.逆转脂质代谢异常:
通过提高细胞内胆碱水平,促进磷脂酰胆碱(PC)的合成。
增强PCYT1B和LPCAT3基因的表达,进一步促进PC的合成与重塑。
提高多不饱和磷脂酰胆碱的比例,优化细胞膜脂质组成。
2.恢复线粒体稳态:
促使线粒体解耦联呼吸恢复正常。
显著降低线粒体膜电位及活性氧(ROS)水平,减少氧化应激。
上调线粒体融合相关基因(如MFN2、OPA1),支持健康的线粒体网络结构,增强线粒体功能。
3.改善AD相关病理表型:
在皮质类器官模型中,观察到β-淀粉样蛋白40(Aβ40)与β-淀粉样蛋白42(Aβ42)的分泌恢复正常。
减少神经元自发性动作电位频率,缓解过度兴奋状态,从而减轻神经毒性。这些发现表明,CDP-胆碱在调节脂质代谢、维持线粒体稳态以及改善AD相关病理方面具有显著的潜力。
五、临床转化
机制创新:建立“脂质-线粒体-神经元兴奋性”轴
本研究首次揭示了ABCA7功能丧失(LoF)导致的代谢和电生理异常通路。具体而言,ABCA7 LoF引发磷脂代谢紊乱,进而改变线粒体膜脂组成,导致线粒体膜电位升高和活性氧(ROS)积累。这些变化最终导致神经元应激和电活动异常,进一步促进β-淀粉样蛋白(Aβ)的累积和神经炎症。该通路将脂质转运、能量代谢和电生理活动串联起来,为理解AD提供了新的框架。
共性机制:罕见与常见变异的汇聚效应
研究发现,罕见的LoF变异和常见的Gly1527变异在转录和功能上存在部分重叠,表明ABCA7功能下调是一个连续谱,而非简单的二元效应。这一发现解释了ABCA7在人群中的广泛影响。
治疗靶点:磷脂代谢作为可干预环节
CDP-胆碱作为一种已获临床使用的神经保护剂和膳食补充剂,具有良好的安全性。本研究为其在AD干预中的应用提供了机制依据和临床前证据。此外,流行病学数据显示高膳食胆碱摄入与低AD风险相关,进一步支持其转化潜力。
六、总结
ABCA7基因是AD的重要风险因子,其功能缺失可通过干扰神经元中的磷脂代谢及线粒体能量稳态,加速神经退行性病变。常见的变异p.Ala1527Gly亦因结构变化而引发类似效应。CDP-胆碱通过促进磷脂酰胆碱(PC)的合成与重塑,部分逆转了上述病理过程,提示靶向磷脂代谢可能成为治疗AD的新策略。未来的研究方向包括:
(1)深入探讨ABCA7在不同磷脂亚型转运中的具体机制
(2)在动物模型及早期AD患者中评估CDP-胆碱的治疗效果
(3)研究ABCA7与其他脂质相关风险基因(如APOE)之间的相互作用
(4)开发基于脂质代谢调控的联合治疗方法本研究不仅增进了对AD遗传学机制的理解,还为临床应用提供了新的潜在靶点和治疗思路。
参考文献
von Maydell D, Wright SE, Pao PC, et al. ABCA7 variants impact phosphatidylcholine and mitochondria in neurons[J]. Nature,2025,647(8089):462-471.




